Auch der Prüfer eines Medizinprodukts kann gegenüber einem Patienten haften, wenn er den Hersteller nicht genug überwacht hat. Was die richtungsweisende Entscheidung des EuGH für Prüfstellen heißt, erklärt Florian Niermeier.
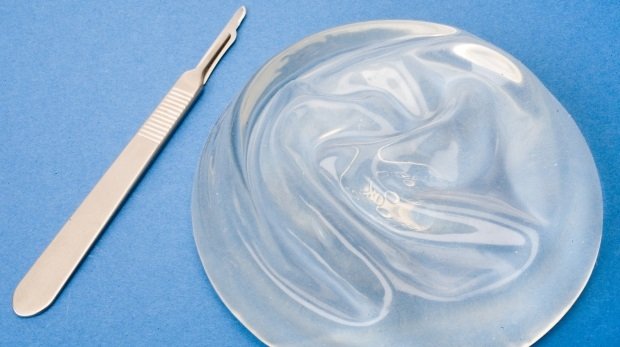
Eine Frau hatte sich in Deutschland Brustimplantate des französischen Herstellers Poly Implant Prothèse (PIP) einsetzen lassen. Diese hatte PIP, wie sich erst später herausstellte, vorsätzlich mit minderwertigem, reißanfälligem Industriesilikon gefüllt. Nachdem französische Behörden das festgestellt hatten, ließ die klagende Patientin wie hunderte anderer Frauen in Deutschland auf ärztliche Empfehlung hin die fehlerhaften Implantate wieder entfernen.
PIP aber war mittlerweile insolvent. So verklagte sie den TÜV Rheinland auf Zahlung von 40.000 Euro Schmerzensgeld sowie auf Feststellung der Ersatzpflicht für ihr künftig durch die fehlerhaften Implantate entstehende Schäden. Der TÜV Rheinland war vom Hersteller als sog. benannte Stelle – das sind staatlich benannte und überwachte Prüfstellen – damit beauftragt, die nach dem Medizinprodukterecht erforderlichen Produktprüfungen vorzunehmen und die Produktion laufend zu überwachen.
Aus Sicht der Klägerin war der TÜV jedoch seinen Prüfungs- und Überwachungspflichten bzgl. der Brustimplantate, die zu den Medizinprodukten mit der höchsten Risikoklasse (III) gehören, nicht hinreichend nachgekommen.
Der Europäische Gerichtshof (EuGH) urteilte am Donnerstag, dass eine benannte Stelle im Rahmen des Medizinprodukterechts zum Schutz der Endempfänger der Medizinprodukte tätig wird, also auch von Patienten haftbar gemacht werden kann. Die Voraussetzungen dafür richten sich aber nach nationalem Recht.
Die benannte Stelle ist nicht generell verpflichtet, Medizinprodukte zu prüfen, Geschäftsunterlagen des Herstellers zu sichten oder unangemeldete Inspektionen durchzuführen. Allerdings bestehe diese Pflicht anlassbezogen, wenn ihr Hinweise darauf vorliegen, dass die Produkte fehlerhaft sind (Urt. v. 16.02.2017, Az. C-219/15).
Was der BGH wissen wollte
Dazu kam es durch eine Vorlage des Bundesgerichtshofs (BGH). Der stellte, nachdem die Klage der Patentin in den Vorinstanzen keinen Erfolg gehabt hatte, dem EuGH drei Fragen zur Auslegung der europäischen Medizinprodukterichtlinie 93/42/EWG (Beschl. v. 09.04.2015, Az. VII ZR 36/14).
Die Karlsruher Richter wollten wissen, ob es Zweck und Intention der Richtlinie ist, dass die mit der Prüfung und Überwachung beauftragte Stelle bei Medizinprodukten der Klasse III zum Schutz aller potentieller Patienten tätig wird, und deshalb bei schuldhafter Pflichtverletzung den betroffenen Patienten unmittelbar und uneingeschränkt haften kann.
Diese erste Vorlagefrage sollte zum einen klären, ob die Patientin über das Rechtsinstitut des Vertrags mit Schutzwirkung zugunsten Dritter in die Schutzpflichten des zwischen PIP und TÜV Rheinland geschlossenen Vertrags einbezogen werden kann. Zum anderen wollte der BGH wissen, ob die einschlägigen medizinprodukterechtlichen Normen ein Schutzgesetz im Sinne des Deliktsrechts darstellen, woraus sich eine Haftung des TÜV Rheinland ergeben kann.
Außerdem fragte der VII. Zivilsenat, ob sich aus der Medizinprodukterichtlinie eine generelle oder zumindest anlassbezogene Produktprüfungspflicht der benannten Stelle ergibt und ob diese generell oder anlassbezogen verpflichtet ist, Geschäftsunterlagen des Herstellers zu sichten und/oder unangemeldete Inspektionen durchzuführen. Damit zielte er auf mögliche Pflichtverletzungen des TÜV Rheinland bei seiner Überwachung des Herstellers PIP ab. Insbesondere könnte, so der Vorwurf der klagenden Patientin, der TÜV entweder die Implantate unzureichend geprüft oder es unterlassen haben, Geschäftsunterlagen seines Auftraggebers PIP zu sichten oder unangemeldete Kontrollen durchzuführen. Und tatsächlich könnte sie damit Recht bekommen.
2/2: EuGH: Wen die benannte Stelle schützt und wie sie das tun muss
Der EuGH folgt mit seinem Urteil vom Donnerstag weitgehend den Schlussanträgen der Generalanwältin vom 15. September 2016 und bejaht im Kern die vom BGH vorgelegten Fragen.
Zur ersten Vorlagefrage stellt der Gerichtshof fest, dass die benannte Stelle im Rahmen des Medizinprodukterechts zum Schutz der Endempfänger der Medizinprodukte tätig wird. Die genauen tatbestandlichen Voraussetzungen einer Haftung der benannten Stelle unterliegen jedoch dem nationalen Recht.
Auf Basis dieser für den BGH verbindlichen Antwort ist eine Haftung des TÜV Rheinland nicht ausgeschlossen. Die klagende Patientin kann in den Schutzbereich des zwischen TÜV und PIP geschlossenen Vertrags einbezogen worden sein; vor allem aber stellen die relevanten Normen des Medizinprodukterechts Schutzgesetze im Sinne des deutschen Deliktsrechts dar.
Die zweite und dritte Vorlagefrage bejaht der EuGH grundsätzlich, aber mit einer Einschränkung. Für die benannte Stelle besteht ausdrücklich keine generelle Pflicht, Medizinprodukte zu prüfen, Geschäftsunterlagen des Herstellers zu sichten oder unangemeldete Inspektionen durchzuführen. Allerdings gibt es eine solche Pflicht anlassbezogen: Wenn die benannte Stelle Hinweise darauf hat, dass ein Medizinprodukt die Anforderungen der Richtlinie möglicherweise nicht erfüllt, muss sie alle erforderlichen Maßnahmen ergreifen, um ihren Verpflichtungen aus der Medizinprodukte-Richtlinie nachzukommen.
Zu diesen anlassbezogenen Pflichten gehört insbesondere, dass sich die benannte Stelle davon überzeugt, dass der Hersteller die Vorgaben seines Qualitätssicherungssystems einhält und dass sie ggf. feststellt, ob die EG-Konformitätserklärung für das Produkt aufrecht erhalten werden kann.
Benannte Stellen sollten Systeme implementieren und dokumentieren
Es ist nun am BGH, zu entscheiden, ob der TÜV Rheinland tatsächlich haftet. Die Karlsruher Richter werden prüfen, ob es Hinweise auf eine Fehlerhaftigkeit der Implantate gab und ob der TÜV Rheinland seine dann bestehenden anlassbezogenen Prüfungspflichten verletzt hat.
Die Folgen des Urteils aus Brüssel gehen weit über den konkreten Einzelfall hinaus. Der EuGH hat sich klar zur rechtlichen Einordnung von Überwachungstätigkeiten benannter Stellen, den Voraussetzungen für eine mögliche Haftung dieser Stellen und zum drittschützenden Charakter des Medizinprodukterechts positioniert. Das werden auch Gerichte anderer EU-Staaten beachten müssen.
Für die Beratung benannter Stellen bedeutet das, dass diese europaweit ihre internen Prozesse daraufhin überprüfen sollten, ob sie mit ihren bestehenden Abläufen den Anforderungen des EuGH gerecht werden. Dabei sollten sie Systeme implementieren, mit denen Hinweise auf eine Nichtkonformität der Produkte erkannt und die erforderlichen weiteren Prüfschritte eingeleitet werden. Wichtig ist auch die Dokumentation dieser Systeme und der im Einzelfall getroffenen Entscheidungen sowie der weiteren Prüfschritte. Benannte Stellen sollten schließlich ihren bestehenden Versicherungsschutz prüfen und ggf. aufstocken.
Ihre Pflichten werden auch unter der künftigen europäischen Medizinprodukteverordnung nicht weniger umfangreich werden. Der Verordnungsentwurf sieht insbesondere auch unangekündigte Inspektionen und stichprobenartige Kontrollen von Medizinprodukten vor. Darauf sollten sich nicht nur die benannten Stellen, sondern auch alle anderen auf dem Feld der Medizinprodukte tätigen Wirtschaftsakteure einstellen.
Der Autor Dr. Florian Niermeier ist Rechtsanwalt bei Noerr LLP in München. Als Mitglied der Praxisgruppen Prozessführung, Schiedsverfahren & ADR sowie Gesundheitswesen ver-tritt er Mandanten in streitigen Verfahren und berät sie zu Fragen des Medizinprodukte-rechts.
Dr. Florian Niermeier , EuGH bejaht Prüferhaftung für Medizinprodukte: Muss der TÜV für fehlerhafte Brustimplantate zahlen? . In: Legal Tribune Online, 16.02.2017 , https://www.lto.de/persistent/a_id/22128/ (abgerufen am: 02.05.2024 )
Infos zum Zitiervorschlag